Depuis 2002, Swissmedic contrôle tous les produits thérapeutiques qui sont commercialisés en Suisse. Leurs expertes et experts indépendants sont responsables de veiller à ce que les produits thérapeutiques dont vous et vos proches avez besoin soient sûrs, efficaces et de grande qualité.
Une brève introduction
Histoire
Swissmedic a commencé ses activités le 1er janvier 2002 en tant que successeur de l'Interkantonale Kontrollstelle für Heilmittel (IKS), qui avait elle-même succédé à la Schweizerische Arzneimittelnebenwirkungszentrale (SANZ).
Le Centre suisse des effets secondaires des médicaments (SANZ) était une fondation privée créée en 1979 à Coire pour enregistrer les effets indésirables des médicaments. Son activité a été reprise en 2001 par l'Institut suisse des produits thérapeutiques Swissmedic, propriété de la Confédération, après l'entrée en vigueur de la loi suisse sur les produits thérapeutiques et une période de transition.
Les fondateurs étaient la Fédération des médecins suisses (FMH, 20%) et scienceindustries. Le dernier budget annuel s'élevait à 450 000 CHF.
Les déclarations reçues de médecins étaient accompagnées d'expertises et évaluées définitivement après avoir complété les données internes des entreprises pharmaceutiques. Les évaluations étaient particulièrement demandées par les médecins et les pharmaciens.
SANZ a été critiqué car la majorité des voix émanait des professions du secteur secondaire : « les cols bleus ».
Aujourd'hui
Swissmedic est une institution publique de la Confédération suisse et une entité juridique à part entière. Elle est organisée et gérée de manière autonome, dispose de son propre budget et gère ses propres comptes. En tant qu'unité administrative décentralisée chargée de tâches de surveillance dans les domaines de l'économie et de la sécurité, elle est rattachée au Département fédéral de l'intérieur. Ses organes statutaires sont le Conseil de l'Agence, le Conseil d'administration et l'organe de révision.
Le Conseil fédéral a désigné Ernst & Young AG (EY) comme organe de révision pour la période de 2020 à 2023.
En tant qu’institut indépendant, Swissmedic peut exercer des droits et contracter des engagements. Il peut par exemple conclure des contrats avec des inspectorats intercantonaux ou des laboratoires.
Swissmedic reçoit entre 12 000 et 15 000 demandes d’AMM par an – qui sont examinées par 150 collaboratrices et collaborateurs au total. Il s’agit notamment de demandes de nouvelles autorisations, d’élargissement des indications ou de modifications de la composition et des méthodes de fabrication. Moins de 2% de ces demandes concernent des vaccins.
À la lecture des rapports annuels et des prévisions de Swissmedic, il apparaît clairement que leur priorité est d'approuver davantage de médicaments en moins de temps. Il est évident que plus ils autorisent de médicaments, plus ils gagnent de l'argent. Les avantages réels pour la santé de la population suisse ne semblent guère être pris en compte.
Environs 16% du budget de Swissmedic provient de la Confédération.
Le reste vient principalement de l'industrie pharmaceutique.
Swissmedic a en effet une double casquette : elle est responsable de l'approbation des médicaments et des dispositifs médicaux sur le marché suisse, mais aussi de la surveillance de la sécurité de ces produits et de leur retrait du marché s'il existe des signaux de sécurité suffisants.
Swissmedic et le Covid-19
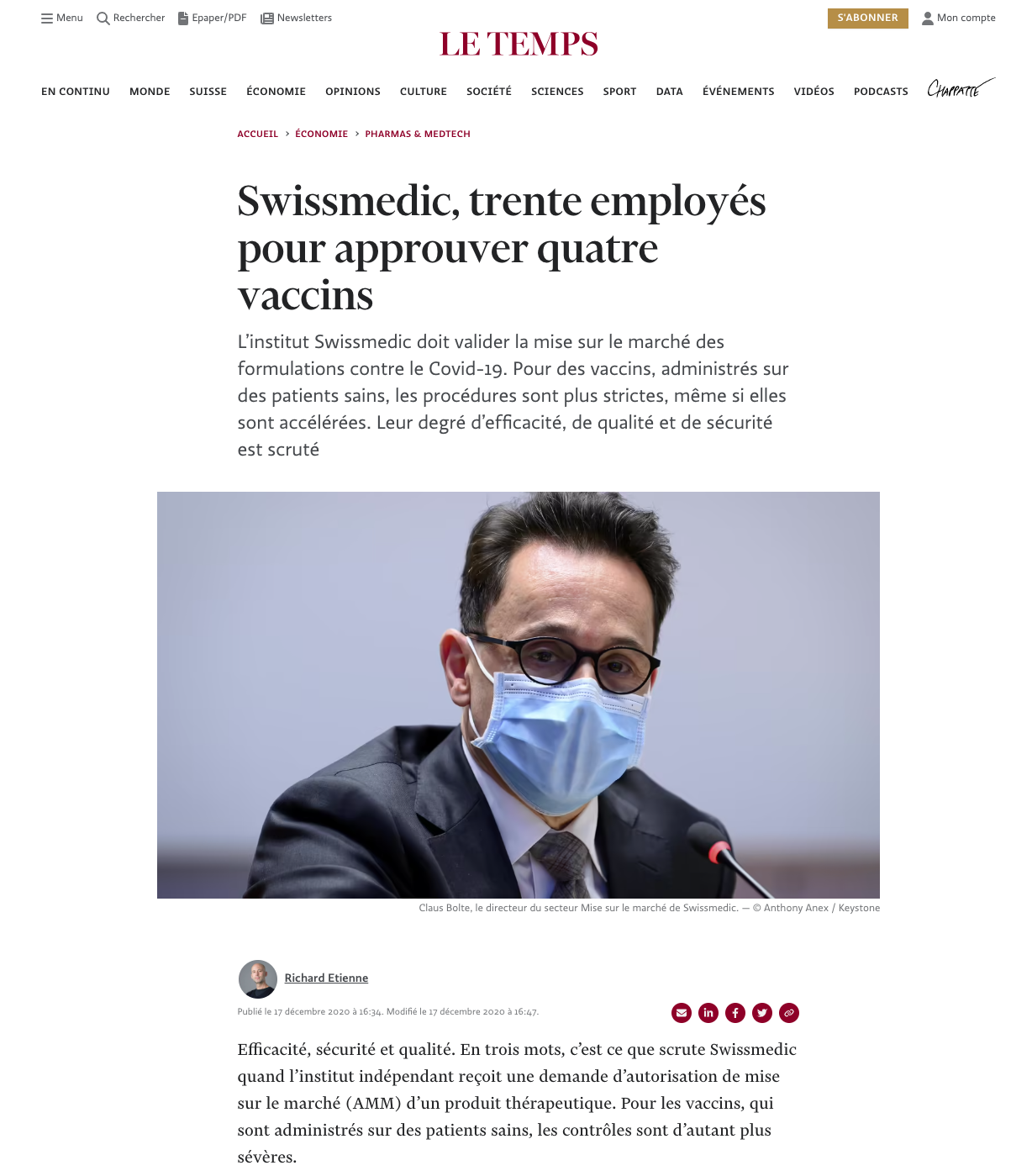
L'article du journal Le Temps, daté le 27 décembre 2020 précise :
« L’efficacité du vaccin doit être aussi élevée que possible. Swissmedic ne fournit pas de chiffre, mais d’autres agences, comme la FDA américaine, l’EMA en Europe et Santé Canada, évoquent le seuil des 50%. Les essais cliniques doivent autrement dit démontrer que le candidat vaccin réduit au minimum de moitié l’incidence de la maladie chez les personnes vaccinées par rapport à un groupe ayant reçu un placebo. »
N'oublions pas que l'allégation marketing d'une efficacité de 95% pour le vaccin Covid-19 de Pfizer était plutôt trompeuse, puisqu'il s'agissait d'un calcul basé sur le risque relatif. Contrairement à la pensée générale, cela ne signifiait pas que la vaccination réduirait le risque d'infection de 95%.
Selon le rapport publié dans le New England Journal of Medicine, lors d'un essai préliminaire de Pfizer portant sur 37 000 participants, 170 d'entre eux ont développé le Covid. Huit d'entre eux faisaient partie du groupe vacciné et 162 du groupe placebo. Les taux d'infection étaient donc de 0,04% contre 0,88%, soit une efficacité relative de plus de 95%. La différence absolue entre les groupes était de 0,84%, ce qui signifie que le vaccin a permis d'éviter une infection par le Covid-19 pour 119 personnes vaccinées, soit une efficacité de moins de 1%.
Ce chiffre est loin d'atteindre le taux d'efficacité minimal de 50% requis pour justifier l'autorisation de ce traitement expérimental.
Rappelons également que, selon l'article 9a LPTh la procédure accélérée d'autorisation à durée limitée, appliquée à tous les produits contre le Covid-19, est censée respecter trois critères :
- Le médicament doit être destiné à la prévention d’une maladie qui peut entraîner une invalidité grave, de grandes souffrances potentiellement mortelles ou la mort à court terme du patient.
Le risque était pour les personnes âgées (moyen d'âge de mortalité était de 83 ans) ou des personnes immunodéprimées avec des co-morbidités tels que l'obésité et le diabète. La grand majorité de la population n'était pas à risque. - Aucun médicament de substitution et équivalent ne doit être autorisé en Suisse.
Cela pourrait expliquer pourquoi les médicaments efficace et bon marché tels que l'hydroxychloroquine et l'ivermectine ont été dénigrés et rendus inaccessibles. - L’utilisation du médicament faisant l’objet de la demande d’autorisation apporte un bénéfice thérapeutique important.
Cela n'a manifestement pas été prouvé et les produits continuent de faire plus de mal que de bien, comme en témoignent les rapports d'effets indésirables qui ne sont pourtant pas suffisamment signalés.
Pour ajouter l'insulte à l'injure, les récents produits de rappel Covid-19 XBB 1,5 de Moderna (dès 18 ans) et Pfizer (dès 12 ans) ont été autorisés en septembre 2023 selon la même procédure que celle appliquée aux vaccins contre la grippe, qui sont sur le marché depuis des dizaines d'années. Cela permet aux fabricants d'obtenir l'autorisation de leurs produits sans avoir effectué les tests d'innocuité et d'efficacité appropriés.
Et bien sûr, la charge de la preuve en cas de préjudice incombe fermement à la victime, toute indemnisation étant de surcroît payée par les contribuables.
Richard Etienne continue dans son article sur Swissmedic que :
« Le fabricant doit apporter la preuve que son produit prévient une infection au SARS-CoV-2 en fournissant des résultats d’essais réalisés sur l’homme.
Les fabricants doivent prouver que leur vaccin est sûr. Il faut pour cela disposer d’une base de données adaptée qui recense les effets secondaires peu fréquents.
Les fabricants doivent respecter les normes internationales, de bonnes pratiques de fabrication, qui visent à garantir que les procédés de fabrication dans chaque usine respectent un standard de qualité. Des données attestant que la stabilité du vaccin a été démontrée doivent également être fournies. »
Est-ce que Swissmedic a respecté ses obligations envers le public suisse, en autorisant ces produits expérimentaux à toute la population, dès 5 ans?
À ce jour—le dernier décompte date de fin juin 2024—plus de 249 décès, et 6 949 effets graves ont été évalués suite à l'administrations des injections anti-Covid-19.
Entre les variations dans la toxicité des lots des vaccins et la contamination de ceux-ci, il semble que Swissmedic ne respecte plus son mandat d'assurer des produits sûrs et efficaces sur le marché suisse.
Lire ci-dessous la mise à jour de la plainte pénale contre Swissmedic
Pour rappel, la campagne de vaccination contre la grippe porcine aux États-Unis en 1976 a été suspendue après 13 décès dans une population de plus de 40 millions personnes vaccinées.
Qui est responsable ?
Christoph Küng
Sécurité des médicaments
Avec plus de 15 ans de carrière professionnelle chez des sociétés pharmaceutique telles que CSL, Solvay, Janssen-Cilag et Rhone-Poulenc-Rorer (Sanofi), il était également membre du comité de l'Association suisse des professionnels de la pharmacie (SwAPP) pendant 4 ans.
Quels sont les conflits d'intérêts et les liens financiers potentiels des salariés de Swissmedic ?
Qui détient des actions et parts de sociétés ?
Qui reçoit des honoraires ?
Nous avons envoyé une lettre à Swissmedic pour demander des précisions...
Voici la réponse rapide reçue de Swissmedic par courriel :
Madame,
Nous nous référons à vos courriers de même teneur du 12 décembre 2023 adressés à Helga Horisberger et Barbara Schütz. Nous nous permettons, puisque vous nous avez communiqué une adresse e-mail, de vous faire parvenir nos réponses par courriel :
Swissmedic dispose d’une ordonnance sur le personnel (RS 812.215.4), sur la base de laquelle le Conseil de l’Institut a adopté un code de conduite. Celui-ci fait partie intégrante du contrat de travail et doit être impérativement respecté par l’ensemble des collaborateurs, y compris le directeur et les membres de la direction. Le code de conduite prévoit notamment l’interdiction de détenir certaines participations, des obligations de déclarer et de soumettre à autorisation des activités accessoires, l’interdiction d’accepter des avantages et règle la gestion d’éventuels honoraires perçus pour des conférences. Le code de conduite est publié sur le site internet de Swissmedic. (Direction (swissmedic.ch)) Les éventuelles activités accessoires des membres de la direction sont énumérées de manière exhaustive dans les CV mis en ligne.
Le règlement du Conseil de l’Institut contient également ce code. Le règlement et les liens d’intérêts des membres du Conseil de l’Institut sont publiés sur le site internet de Swissmedic. (Conseil de l'institut (swissmedic.ch))